Dutasteride
- μέγεθος γραμματοσειράς μείωση του μεγέθους γραμματοσειράς αύξηση μεγέθους γραμματοσειράς
- Εκτύπωση
- Επιστημονική επιμέλεια κειμένου: Dr. Κωνσταντίνος Αναστασάκης MD, PhD, FISHRS, ABHRS Secretary, Χειρουργός Κεφαλής & Τραχήλου
Το Dutasteride είναι ένα φαρμακευτικό μόριο παρόµοιο σε χηµική µορφή µε το Finasteride µε µια σηµαντικότατη διαφορά: είναι εκλεκτικός αναστολέας και των δύο ισοτύπων του ενζύµου 5-α-αναγωγάση, δηλαδή των ισοτύπων Ι και ΙΙ.
Η 5-α-αναγωγάση μετατρέπει την «ανδρική ορμόνη» Τεστοστερόνη σε μία μορφή που επιδρά αρνητικά στα τριχοθυλάκια, την Διυδροτεστοστερόνη, DHT. Η DHT έχει την ιδιότητα να προκαλεί αλλαγές στα τριχοθυλάκια σε συγκεκριμένες περιοχές του τριχωτού: υπό την επίδραση της DHT τα τριχοθυλάκια σταδιακά συρρικνώνονται, οι τρίχες μεγαλώνουν πιο αργά, χάνουν το χρώμα τους και τελικά τα τριχοθυλάκια καταλήγουν να παράγουν μόνο ξανθό χνούδι.
Συγκεκριµένα, είναι ο πρώτος και µοναδικός µέχρι σήµερα διπλός αναστολέας του ενζύµου 5α-R, µε το οποίο συνδέεται ισχυρά, δηµιουργώντας ένα σταθερό σύµπλεγµα που διαλύεται εξαιρετικά αργά, µην επιτρέποντας στην Τεστοστερόνη να ενωθεί µε το 5α-R και να µετατραπεί σε DHT.
Ενώ το Finasteride αναστέλλει τον ισότυπο 5α-R ΙΙ κατά 70% και σε αµελητέο βαθµό τον ισότυπο Ι, το Dutasteride βρέθηκε να είναι 2 φορές πιο ισχυρό από το Finasteride στην αναστολή του 5α-R ΙΙ και 45 φορές πιο ισχυρό στην αναστολή του 5α-R Ι.
Από την αρχή της ανακάλυψής του Dutasteride υπήρξε ενδιαφέρον για τη χρήση του σε ασθενείς µε ΑΓΑ µε σκοπό να µελετηθεί αν το Dutasteride µπορεί να ακολουθήσει το παράδειγµα του Finasteride και να αποτελέσει µια επιπλέον αποτελεσµατική αγωγή ενάντια στην ΑΓΑ.
Το Dutasteride δεν έχει εγκριθεί από τον Αμερικανικό Οργανισμό Φαρμάκων και Τροφίμων (Food and Drug Administration, FDA) με ένδειξη ενάντια στην τριχόπτωση που προκαλείται από ΑΓΑ. Εκτελούνται ακόμα κλινικές μελέτες προκειμένου να διαπιστωθεί η ασφάλεια και η αποτελεσματικότητα της ουσίας στην αντιμετώπιση της ΑΓΑ.
Για περισσότερες λεπτομέρειες για το Dutasteride διαβάστε παρακάτω
Dutasteride (εμπορική ονομασία Avodart®)
Χορήγηση
Από το στόμα κάψουλες, δοσολογία 0,5mg. Με την εμπορική ονομασία Avodart ® χρησιμοποιείται σε δοσολογία 0,5mg για την αντιμετώπιση της καλοήθους υπερτροφίας του προστάτη (ΚΥΠ).
Διαθεσιμότητα
Γενικά, στις περισσότερες χώρες απαιτείται συνταγογράφηση. Το Dutasteride έχει εγκριθεί από τους αρμόδιους Κρατικούς και Επιστημονικούς φορείς για την αντιμετώπιση της ΚΥΠ στους άνδρες. Είναι σε εξέλιξη κλινικές μελέτες προκειμένου να λάβει το Dutasteride την έγκριση των αρμόδιων φορέων ως αγωγή και για την ανδρική Ανδρογενετική Αλωπεκία.
Σε κάποιες Ευρωπαϊκές χώρες έχει εγκριθεί, σε διαφορετική δοσολογία από το 0,5mg για την αντιμετώπιση της τριχόπτωσης. Ιατροί στις ΗΠΑ κάποιες φορές συνταγογραφούν το Dutasteride για χρήση εκτός της προβλεπόμενης (off-label), για αντιμετώπιση της ανδρικής Ανδρογενετικής Αλωπεκίας εφόσον τα χαρακτηριστικά ενός μεμονωμένου ασθενή επιτρέπουν τέτοια χρήση.
Τρόπος δράσης
Η καινοτοµία του Dutasteride βασίζεται στην ιδιότητα να αναστέλλει συνολικά και πλήρως το ενζυµικό σύστηµα του ενζύμου της 5-α-αναγωγάσης. Το Dutasteride είναι εκλεκτικός αναστολέας και των δύο ισοτύπων του ενζύµου 5-α-αναγωγάση. Είναι 2 φορές πιο ισχυρό από το Finasteride στην αναστολή του ενζύμου 5α-R ΙΙ και 45 φορές πιο ισχυρό στην αναστολή του τύπου Ι.
Αποτελεσματικότητα
Ενώ το Dutasteride έχει εγκριθεί για την αντιμετώπιση της ΚΥΠ και έχει αποδεδειγμένα θετική δράση ενάντια στην ΑΓΑ, εντούτοις δεν έχει λάβει ακόµα επίσημη έγκριση από το FDA µε ένδειξη ενάντια στην ΑΓΑ. Σε κλινικές μελέτες που έχουν φτάσει μέχρι το Phase II (για έγκριση απαιτείται και η Phase III), το Dutasteride έχει δείξει παρόμοια και ενίοτε και ανώτερη αποτελεσματικότητα από το Finasteride στην αντιμετώπιση της Ανδρογενετικής Αλωπεκίας, χωρίς σημαντικά αυξημένες παρενέργειες σε σύγκριση με το Finasteride.
Συγκεκριμένα, το 1999 συντάχθηκε η Dutasteride Alopecia Research Team, µε εξέχοντες Δερµατολόγους και Ουρολόγους και σχεδιάστηκε το πρωτόκολλο της µελέτης µικρής κλίµακας σε ανθρώπους (Phase ΙΙ). Σε αυτή την πολυκεντρική (21 κέντρα) διπλή-τυφλή µελέτη, συµπεριλήφθηκαν 416 άνδρες ηλικίας 21-45 ετών που ανήκαν στα στάδια κατά Norwood-Hamilton III vertex - V και έγινε ταυτόχρονη σύγκριση µε placebo και Finasteride 5mg (Proscar®). Αποδείχθηκε πως η δόση 0,1mg Dutasteride (1/5 της δόσης που χρησιµοποιείται ενάντια στην ΚΥΠ) είχε παρόµοια αποτελεσµατικότητα στην ανάπτυξη τριχών και στη µείωση της DHT στον ορό µε τη δόση 5mg Finasteride, ενώ τα µέγιστα αποτελέσµατα στην τριχοφυΐα επιτυγχάνονταν µε δοσολογία Dutasteride 2,5mg. Ενώ, λοιπόν, το Dutasteride φάνηκε πολλά υποσχόµενο στην αντιµετώπιση της ΑΑ και η GlaxoSmithKline είχε ανακοινώσει το χρονοδιάγραµµα για την έναρξη των µελετών µεγάλης κλίµακας Phase ΙΙΙ, αποφάσισε να τις αναβάλει για άγνωστους λόγους. (Σχήμα 1)
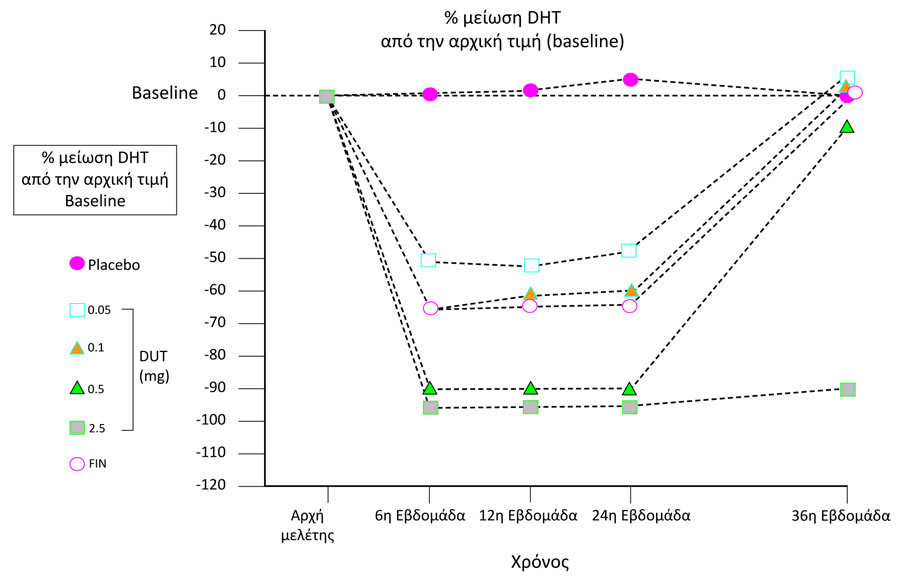
Σχήμα 1. Γράφημα μείωσης της DHT στη διάρκεια της μελέτης. Το Dutasteride 2,5mg συνεχίστηκε και μετά τις 24 εβδ. Και φυσικά διατήρησε τα θετικά αποτελέσματα στα μαλλιά των ασθενών.
Αποτέλεσµα της αρχικής αναβολής των µελετών Phase III είναι ότι, ενώ το Dutasteride έχει εγκριθεί για την αγωγή της ΚΥΠ και έχει αποδεδειγµένη δράση ενάντια στην ΑΓΑ, δεν έχει ακόµα έγκριση από το FDA µε ένδειξη ενάντια στην ΑΓΑ. Εντούτοις, το Φεβρουάριο του 2007, η GlaxoSmithKline προχώρησε σε μια αρχική µελέτη Phase ΙΙΙ που ολοκληρώθηκε τον Ιανουάριο του 2008 και τα αποτελέσµατα ανακοινώθηκαν τον Αύγουστο του 2010. Η εκτίµηση τόσο των ερευνητών όσο και των ασθενών ήταν σηµαντικά θετικότερη για την οµάδα που έλαβε την ενεργή ουσία µετά την πάροδο 6 µηνών και µόλις 3 από τους 73 ασθενείς (4,1%) υπό Dutasteride ανέφεραν κάποια παρενέργεια, ενώ 2 από τους 75 ασθενείς στην οµάδα placebo ανέφεραν Σεξουαλικές Δυσλειτουργίες (2,7%). Αναµένεται επέκταση της µελέτης σε πολύκεντρική µελέτη παρακολούθησης σε 900 άνδρες µε ΑΓΑ και ολοκλήρωση των αποτελεσµάτων µε εποπτεύοντα οργανισµό τον Κορεατικό FDA.
Σε μελέτη του 2014 που συνέκρινε το Dutasteride 0,5mg µε το Finasteride (1mg) σε 917 άνδρες 20-50 ετών αποδείχθηκε πως το Dutasteride υπερείχε σε κάθε µέτρηση από το Finasteride και το placebo, ενώ έδωσε θετικά αποτελέσµατα και στην πρόσθια περιοχή, χωρίς σηµαντικά περισσότερες παρενέργειες.
Παρενέργειες
Το προφίλ ανεπιθύµητων ενεργειών του Dutasteride είναι παρόµοιο µε του Finasteride και αναφέρονται Σεξουαλικές Δυσλειτουργίες που όµως είναι σπάνιες (<4%) και αυτοπεριοριζόµενες, ακόμα και με τη συνέχιση της αγωγής. Όπως και με το Finasteride, το Dutasteride δεν πρέπει να χορηγείται σε γυναίκες που είναι έγκυες ή μπορεί να μείνουν έγκυες. Οι παρενέργειες του Dutasteride είναι παρόμοιες με αυτές που έχουν καταγραφεί για το Finasteride, όπως μειωμένη libido (διάθεση για sex), στυτική δυσλειτουργία, διόγκωση του ανδρικού στήθους και κατάθλιψη.
Ανεπίσηµα, και άλλες ανεπιθύµητες ενέργειες έχουν αναφερθεί από άτοµα που κάνουν χρήση Dutasteride για την ΑΓΑ, όπως κεφαλαλγία, διαταραχές ύπνου και συµπεριφοράς, γαστρικές διαταραχές, ξηρότητα τριχωτού και δέρµατος προσώπου και µειωµένη ανάπτυξη τριχοφυΐας σώµατος.
Αλληλεπιδράσεις φαρμάκων που έχουν καταγραφεί αναφέρουν ότι το Dutasteride παρεμβαίνει στη δράση κάποιων αντιβιοτικών, κάποιων αντικαταθλιπτικών και κάποιων φαρμάκων ενάντια στο άγχος και σε κάποια φάρμακα που χρησιμοποιούνται για την αντιμετώπιση του HIV/AIDS. Συγκεκριμένα, αλληλεπιδράσεις έχουν βρεθεί με τις ουσίες Cimetidine, Ciprofloxacin, Ketoconazole, και Verapamil.
Περίληψη
Η σύσταση λήψης Dutasteride ενάντια στην ΑΓΑ είναι στην κρίση του ιατρού, καθότι δεν υπάρχει ακόµα επίσημη έγκριση από τον Αμερικανικό Οργανισμό Φαρμάκων και Τροφίμων (Food and Drug Administration, FDA) με ένδειξη ενάντια στην τριχόπτωση που προκαλείται από ΑΓΑ. Υπάρχουν όµως µελέτες που αποδεικνύουν την εξαιρετική αποτελεσµατικότητα και ασφάλεια του Dutasteride στην ΑΓΑ. Ο ιατρός πρέπει να είναι σε εγρήγορση για εµφάνιση παρενεργειών. Επίσης, ο συνδυασµός του Dutasteride µε εγκεκριµένες φαρµακευτικές ουσίες ενάντια στην ΑΓΑ έχει ενδιαφέρον και δεν είναι λάθος να δοκιµάζεται σε συνεννόηση με τον ιατρό, αν έχει εμπειρία με αυτή την πρακτική. Συγκεκριµένα, η τοπική λοσιόν Dutasteride, σε συνδυασµό µε per os Finasteride πιθανόν να έχει ιδανικά αποτελέσµατα.
Επιστημονική επιμέλεια κειμένου:
Dr. Κωνσταντίνος Αναστασάκης MD, PhD, Χειρουργός Κεφαλής & Τραχήλου, Ωτορινολαρυγγολόγος
Διδάκτωρ Ιατρικής Σχολής Δημοκρίτειου Παν/μιου
Diplomate of the American Board of Hair Restoration Surgery, ABHRS
Βιβλιογραφία
Κωνσταντίνος Αναστασάκης, Ανδρογενετική Αλωπεκία, από το Α ως το Ω. - 1η έκδοση - Αθήνα 2015, Εκδόσεις Γ. ΖΕΒΕΛΕΚΑΚΗΣ και ΣΙΑ ΕΕ., 874 σελίδες. ISBN 978-618-81608-0-4
Ηλεκτρονικές Πηγές
Κύρια πηγή κειμένου: www.ishrs.org (ημερομηνία προσπέλασης 1-8-2016)